Kohlenstoff im Ozean
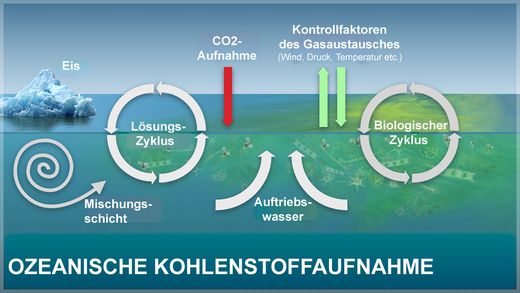
Der Kohlenstoff im Ozean bildet einen eigenen Kreislauf, der Teil des gesamten Kohlenstoffkreislaufs ist, und sich mit dem Terrestrischen Kohlenstoffkreislauf und dem Kohlendioxid in der Atmosphäre austauscht. Der Austausch mit der Atmosphäre beeinflusst stark deren Kohlendioxid-Konzentration.
Die ozeanische Deckschicht
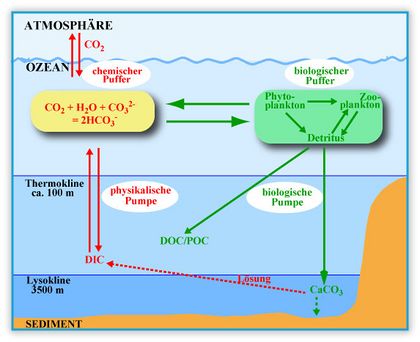
Die gesamte im Ozean gelöste Menge an Kohlenstoff ist etwa 42 Mal größer als jene in der Atmosphäre und 10 Mal größer als der an Land (Vegetation und Böden) gespeicherte Kohlenstoff.[1] Der Ozean tauscht Kohlendioxid (CO2) mit der Atmosphäre aus und fungiert bei einer steigenden CO2-Konzentration in der Atmosphäre über längere Zeiträume als wichtige CO2-Senke (Abb. 2). Der CO2-Austausch mit der Atmosphäre findet über die ozeanische Deckschicht statt, die je nach Region zwischen 50 und mehreren 100 m dick ist. Er wird hauptsächlich durch die Differenz im CO2-Partialdruck zwischen Ozean und Atmosphäre angetrieben. Ist der CO2-Druck in der Atmosphäre niedriger als im Ozean, gast der Ozean Kohlenstoff (in Form von CO2) in die Atmosphäre aus, bei einem höherem CO2-Druck in der Atmosphäre wird Kohlendioxid im Oberflächenwasser des Ozeans aufgenommen. Der zunehmende atmosphärische CO2-Gehalt durch menschliche Emissionen erhöht daher die Aufnahme von Kohlendioxid durch den Ozean.
Gelöstes Kohlendioxid
Die für den Austausch zwischen Atmosphäre und Ozean entscheidenden Eigenschaften von Kohlendioxid sind seine leichte Löslichkeit und seine chemische Reaktivität im Wasser. Die Löslichkeit ist bestimmt durch Temperatur, Salzgehalt, Luftdruck, windabhängige Durchmischung und anderen Faktoren, wobei die Temperatur den größten Einfluss besitzt. Die durch menschliche Emissionen von Treibhausgasen verursachte Erwärmung der Atmosphäre erwärmt auch das Wasser der Ozeane. Wasser mit höherer Temperatur kann weniger Kohlenstoff aufnehmen als Wasser mit geringerer Temperatur. Die globale Erwärmung wirkt daher der Aufnahme von Kohlendioxid durch den unterschiedlichen CO2-Partialdruck entgegen. Hinzu kommt, dass das wärmere Oberflächenwasser weniger stark in die Tiefe absinkt, wodurch auch weniger CO2 aus den oberen Schichten in die Tiefe des Ozeans transportiert wird. Meeresströmungen werden aber nicht nur durch Temperaturunterschiede angetrieben, sondern auch durch Wind und Unterschiede im Salzgehalt.[2]
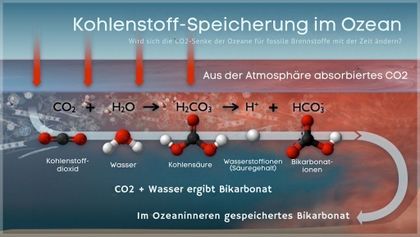
Chemischer Puffer
Die chemische Reaktivität im Wasser ist die zweite wichtige Eigenschaft von Kohlendioxid im Meerwasser. In der Atmosphäre reagiert CO2 nicht mit anderen Molekülen; es ist chemisch inert. Das ist im Meerwasser ganz anders (Abb. 3). Der allergrößte Teil des Kohlendioxids, das im Meerwasser gelöst wird, reagiert chemisch mit Wassermolekülen zu Kohlensäure (H2CO3), Hydrogenkarbonat (HCO3) und Karbonat (CO3). Die wichtigste Verbindung ist Hydrogenkarbonat, in dem 90% des im Ozean gespeicherten Kohlenstoffs gebunden sind.[3] 8% sind als Karbonat (CO32-) gespeichert und nur 1% als physikalisch gelöstes CO2. Bei der Aufnahme von Kohlendioxid aus der Atmosphäre wird das Gas also fast vollständig in andere Verbindungen umgewandelt. Das hat den positiven Effekt, dass der Ozean weiteres CO2 aus der Atmosphäre aufnehmen kann. Die Konzentration von Karbonat, das in geringen Mengen aus der Verwitterung an Land über die Flüsse nachgeliefert wird, ist allerdings eine kritische Größe für die CO2-Aufnahmekapazität des Ozeans. Da ein steigender CO2-Gehalt der Atmosphäre auch die Aufnahme von Kohlendioxid im Ozean erhöht, wird bei den chemischen Lösungsvorgängen auch mehr Karbonat verbraucht, und es steht zunehmend weniger Karbonat für die chemische Reaktion mit Kohlendioxid zur Verfügung. Weniger chemische Umwandlung bedeutet, dass mehr CO2 im gelösten Zustand in der Deckschicht verbleibt, wodurch diese weniger Kohlendioxid aus der Atmosphäre aufnehmen kann.
Die Entstehung von Kohlensäure durch die Reaktion von CO2 mit Meerwasser ist zudem mit einem erheblichen Problem für zahlreiche Lebewesen im Meer verbunden, vor allem für diejenigen, die Kalkschalen bilden, nämlich der Ozeanversauerung. Die Ozeanversauerung bewirkt eine zunehmende Untersättigung des Ozeanwassers mit Karbonat-Ionen, wodurch es zur Auflösung von Kalkschalen kommen kann.[4]
Biologischer Puffer
Das in der ozeanischen Deckschicht gelöste atmosphärische Kohlendioxid wird aber nicht nur chemisch verwandelt, sondern auch durch die Photosynthese des Phytoplanktons gebunden. Der Kohlenstoff wird dabei in Form von Kohlendioxid oder Hydrogenkarbonat aufgenommen. Das verringert den Partialdruck von CO2 in der oberen Wasserschicht und fördert damit die Aufnahme von Kohlendioxid aus der Atmosphäre. Die Bruttoprimärproduktion durch das ozeanische Phytoplankton wird auf 103 GtC pro Jahr geschätzt, die Veratmung (autotrophe Respiration) auf 58 GtC und die Nettoprimärproduktion entsprechend auf 45 GtC pro Jahr. Der daraus resultierende und im Phytoplankton gebundene organische Kohlenstoff wird vom Zooplankton konsumiert, wobei durch heterotrophe Respiration 34 GtC pro Jahr wieder frei gesetzt werden. Der Rest wird direkt oder indirekt zu Abfall (Detritus) und sinkt für längere Zeit in größere Tiefen ab.
Durch die physikalischen, chemischen und biologichen Prozesse im Ozean ergeben sich drei Arten von Kohlenstoffverbindungen (Abb. 1):
- gelöster anorganischer Kohlenstoff (dissolved inorganic carbon = DIC),
- gelöster organischer Kohlenstoff (dissolved organic carbon = DOC) und
- partikulärer organischer Kohlenstoff (particulate organic carbon = POC).
Die überwiegende Mehrheit ist davon gelöster anorganischer, gefolgt von gelöstem organischen Kohlenstoff. DIC, DOC und POC stehen etwa im Verhältnis 2000:38:1.[5]
Der tiefe Ozean
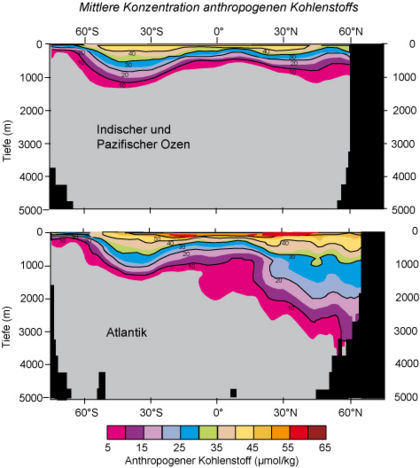
Unterhalb der ozeanischen Deckschicht nimmt die Konzentration des gelösten anorganischen Kohlenstoffs deutlich zu. Die Ursache liegt in zwei fundamentalen Prozessen im Innern des Ozeans: der "physikalischen Pumpe" und der "biologischen Pumpe". Bei der physikalischen Pumpe wird CO2 durch absinkende Wassermassen in die Tiefe verfrachtet, bei der biologischen Pumpe durch das Absinken von organischen Substanzen, in denen Kohlenstoff gebunden ist.
Die physikalische Pumpe
Die Wirkung der physikalischen Pumpe hängt u.a. von der thermohalinen Zirkulation ab. Da CO2 in kaltem Waser besonders gut löslich ist, wird der Transport von atmosphärischem Kohlendioxid in den tieferen Ozean vor allem durch die Bildung von kaltem Wasser mit hoher Dichte im Nordatlantik und dem Gebiet des Antarktischen Zirkumpolarstroms kontrolliert. Mit dem Absinken großer Wassermassen in die Tiefe und ihrer weiteren Ausbreitung über große Entfernungen, z.T. über alle Ozeane, wird das CO2 effektiv und über lange Zeiträume von Jahrzehnten bis Jahrhunderten dem Austausch mit der Atmosphäre entzogen. Das heißt aber auch, dass eine Störung des innerozeanischen Kohlenstoff-Gleichgewichts durch zusätzliche CO2-Aufnahme aus der Atmosphäre erst über Zeiträume von bis zu 1000 Jahren, der Umwälzzeit des Ozeans durch die thermohaline Zirkulation, wieder ausgeglichen werden kann. Die langen Austauschzeiten sind vor allem darin begründet, dass sich erstens die Wassermassen der ozeanischen Tiefenströmungen nur sehr langsam bewegen und zweitens in großen Teilen des Ozeans eine wärmere und leichtere Deckschicht das Aufsteigen von Tiefenwasser verhindert.
Durch den globalen Klimawandel wird auch das Oberflächenwasser des Ozeans erwärmt, und es bilden sich weniger kalte Wassermassen, die in die Tiefe absinken könnten. Dadurch wird der Transport von Kohlenstoff in den tieferen Ozean durch die "physikalische Pumpe" reduziert. Durch den kombinierten Effekt von 1. der zunehmenden chemischen Sättigung des Oberflächenwassers und 2. der zunehmenden Schichtung der Wassersäule werden zwei wichtige negative Rückkopplungen im Kohlenstoff-Klima-System geschwächt und damit die Rate der Aufnahme von anthropogenem Kohlenstoff durch den Ozean reduziert. Die Größenordnung ist entscheidend davon abhängig, wie die ozeanische Zirkulation und die chemische Mischung auf den klimatischen Antrieb reagieren.
Die biologische Pumpe
Das durch die Photosynthese erzeugte organische Material sinkt als Gewebepartikel (particulate organic carbon = POC) in größere Tiefe und wird dort remineralisiert, d.h. in seine Bestandteile aufgelöst. Dieser Abwärtsfluss von organischem Kohlenstoff aus dem oberen Ozean, der etwa 25% des Kohlenstoffs, der im oberen Ozean durch Photosynthese gebunden wird, ausmacht, wird als "biologische Pumpe" bezeichnet und wird gegenwärtig auf etwa 11 Gt C pro Jahr geschätzt. Nur ein minimaler Teil sinkt in das Sediment ab, hauptsächlich im Küstenbereich. Der restliche organische Kohlenstoff wird im tiefen Ozean durch Zersetzung in gelösten anorganischen Kohlenstoff (DIC) zurückverwandelt, der durch aufsteigendes Wasser wieder an die Oberfläche gelangt. Insgesamt sorgt die biologische Pumpe dafür, dass die atmosphärische CO2-Konzentration 150-200 ppm unter dem Wert liegt, der ohne das ozeanische Phytoplankton herrschen würde.
Änderungen des Austauschs zwischen Ozean und Atmosphäre

Regionaler Austausch
Regional sind die mittleren Breiten und besonders der nördliche Nordatlantik die wichtigsten CO2-Senken des Ozeans (Abb. 5). Hier erleichtern niedrige Temperaturen und hohe Windgeschwindigkeiten die CO2-Aufnahme an der Meeresoberfläche. Außerdem befördert die Bildung von Tiefenwasser das anthropogene CO2 in das Innere des Ozeans, wodurch neues Kohlendioxid an der Oberfläche aus der Atmosphäre aufgenommen werden kann. Das Ausgasen von CO2 aus dem Ozean geschieht dagegen hauptsächlich in den Tropen, besonders in den äquatorialen Auftriebsgebieten, und daneben im Nordpazifik und im polaren südlichen Ozean.[1]
Aktuelle Änderungen
Seit 1850 hat die ozeanische Kohlenstoffsenke 185 GtC aufgenommen, was 26% der anthropogenen Emissionen entspricht. Mehr als Zweidrittel davon (130 GtC) erfolgten nach 1960. In den letzten 60 Jahren hat sich die ozeanische Kohlenstoffsenke mehr als verdreifacht. Sie betrug in den 1960er Jahren 1,2 GtC pro Jahr, im letzten Jahrzehnt (2014-2023) dagegen 2,9 GtC pro Jahr. Damit nahm der Ozean über einen längeren Zeitraum 25% der anthropogenen CO2-Emissionen auf. Es gibt bis jetzt keine Anzeichen eines Rückgangs der ozeanischen Kohlenstoffsenke. Der Hauptgrund für die Zunahme der ozeanischen Kohlenstoffsenke ist die Erhöhung der CO2-Konzentration in der Atmosphäre. Der globale Temperaturanstieg schwächt dagegen die ozeanische Senke um 0,17 GtC pro Jahr etwas ab. Grund dafür ist eine Erwärmung des Ozeans, wodurch weniger CO2 im Wasser gelöst wird.[1]
Die Ozeansenke zeigt deutliche dekadische Schwankungen, deren Ursachen aber nicht endgültig geklärt sind. Die ebenfalls beträchtlichen jährlichen Schwankungen werden hauptsächlich durch El-Niño- und La-Niña-Ereignisse verursacht. So hat der El Niño 2015/16 eine Intensivierung der ozeanischen Senke bewirkt, die anschließende La Niña dagegen eine Reduzierung der Senke. Auch das El-Niño-Jahr 2023 zeigt eine Zunahme der ozeanischen Senke.[1]
Zukünftige Änderungen
Nach Modellprojektionen wird die Ozeansenke ab Mitte des Jahrhunderts abnehmen, besonders bei hohen Szenarien. Grund ist vor allem die Erwärmung des Ozeans, die die CO2-Löslichkeit und damit die Aufnahme aus der Atmophäre reduziert und die ozeanische Schichtung erhöht, wodurch der Austausch zwischen der oberen Ozeanschicht und dem Inneren abgeschwächt wird. Auch die chemischen und biologischen Puffer werden bei höheren Temperaturen geringer. Regional ist es sehr wahrscheinlich, dass die abnehmende Nordatlantische Umwälzzirkulation die Aufnahme von Wärme und Kohlenstoff reduziert und damit die globale Erwärmung verstärkt. Im Südlichen Ozean wird nach Modellprojektionen die Umwälzzirkulation dagegen durch stärkere Westwinde intensiver und die Wärme- und Kohlenstoffaufnahme und -speicherung zunehmen.[7]
Einzelnachweise
- ↑ 1,0 1,1 1,2 1,3 Friedlingstein, P., M. O'Sullivan, M.W. Jones et al. (2025): Global Carbon Budget 2024, Earth Syst. Sci. Data, 17, 965–1039, https://doi.org/10.5194/essd-17-965-2025
- ↑ IPCC AR6 WGI (2021): Global Carbon and other Biogeochemical Cycles and Feedbacks, 5.4.4
- ↑ CDRmare (2023): Der natürliche Kohlenstoffkreislauf der Erde – Kohlenstoffspeicher Ozean: So nimmt das Meer Kohlendioxid auf
- ↑ IPCC AR6 WGI (2021): Global Carbon and other Biogeochemical Cycles and Feedbacks, 5.3
- ↑ IPCC (2007): Climate Change 2007, Working Group I: The Science of Climate Change, 7.3.4.1
- ↑ Die Abb. zeigt zwar nur die Kohlenstoffflüsse der anthropogenen fossilen Emissionen. Die Verteilung der Quellen und Senken und die Vorzeichen gelten aber prinzipiell auch für die natürlichen Flüsse.
- ↑ IPCC AR6 WGI (2021): Global Carbon and other Biogeochemical Cycles and Feedbacks, Cross-Chapter Box 5.3
Weblinks
Literatur
- Liebezeit, G. (2011): Meereschemie und globaler Klimawandel, in: José L. Lozán et al. (Hrsg.): Warnsignal Klima: Die Meere - Änderungen und Risiken. Wissenschaftliche Auswertungen, Hamburg, 3236
Lizenzhinweis
| Dieser Artikel ist ein Originalartikel des Klima-Wiki und steht unter der Creative Commons Lizenz Namensnennung-Weitergabe unter gleichen Bedingungen 3.0 Deutschland. Informationen zum Lizenzstatus eingebundener Mediendateien (etwa Bilder oder Videos) können in den meisten Fällen durch Anklicken dieser Mediendateien abgerufen werden und sind andernfalls über Dieter Kasang zu erfragen. |