Ozon: Unterschied zwischen den Versionen
K →Weblinks: typo |
Anja (Diskussion | Beiträge) |
||
| Zeile 14: | Zeile 14: | ||
* Durch ein Gewitter: Durch den elektrischen Stromfluss zwischen Wolke und Erdboden bei der Blitzentladung entsteht Ozon (aber auch Salpetersäure und andere Stoffe). | * Durch ein Gewitter: Durch den elektrischen Stromfluss zwischen Wolke und Erdboden bei der Blitzentladung entsteht Ozon (aber auch Salpetersäure und andere Stoffe). | ||
== Vorkommen == | == Vorkommen und Entstehung von Ozon == | ||
=== Stratosphärisches Ozon === | === Stratosphärisches Ozon === | ||
* Hauptartikel: [[Stratosphärisches Ozon]] | * Hauptartikel: [[Stratosphärisches Ozon]] | ||
| Zeile 22: | Zeile 22: | ||
=== Troposphärisches Ozon === | === Troposphärisches Ozon === | ||
* Hauptartikel: [[Troposphärisches Ozon]] | * Hauptartikel: [[Troposphärisches Ozon]] | ||
In der Atemluft ist | In der Atemluft ist Ozon jedoch bereits in weit geringeren Konzentrationen gesundheitsschädlich, insbesondere bewirkt die lokal sehr unterschiedliche Ozonbelastung Reizungen der Atemwege. | ||
== Ozonabbau == | == Ozonabbau == | ||
Version vom 14. Dezember 2008, 17:50 Uhr
Ozon (O3)(griechisch "das Richende") ist ein aus drei Sauerstoffatomen bestehendes, instabiles Molekül, das innerhalb kurzer Zeit zu dimerem ("normalem") Sauerstoff (O2) zerfällt. Es ist ein starkes Oxidationsmittel.
Eigenschaften
Ozon ist bei Zimmertemperatur und normalem Luftdruck gasförmig. Aufgrund seiner oxidierenden Wirkung ist es für den Menschen giftig. Bei Ozonaufnahme treten beim Betroffenen häufig heftige Kopfschmerzen auf. In hohen Konzentrationen riecht das Gas aufgrund der oxidierenden Wirkung auf die Nasenschleimhaut charakteristisch stechend-scharf bis chlorähnlich, während es in geringen Konzentrationen geruchlos ist. Die Geruchsschwelle liegt bei 40 µg/m3, allerdings gewöhnt man sich schnell an den Geruch und nimmt ihn dann nicht mehr wahr.
Bildung
Ozon entsteht aus gewöhnlichem Sauerstoff gemäß der Grundgleichung
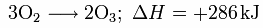
wobei ΔH die molare Reaktionsenthalpie bezeichnet.
Ozon bildet sich in der Atmosphäre vor allem auf drei Arten:
- Energiereiche Sonnenstrahlung spaltet Sauerstoff-Moleküle in der Stratosphäre in zwei einzelne Atome, die sich jeweils mit einem weiteren Sauerstoff-Molekül zu Ozon vereinigen. Dieser Vorgang der Spaltung von Sauerstoff-Molekülen durch energiereiche UV-C-Strahlung mit einer Wellenlänge von < 0,242 µm wird als Photodissoziation bezeichnet.
- In Erdnähe bildet sich Ozon aus einer Reaktion zwischen Stickstoffdioxid NO2 und Sauerstoff O2 unter dem Einfluss von UV-Strahlung.
- Durch ein Gewitter: Durch den elektrischen Stromfluss zwischen Wolke und Erdboden bei der Blitzentladung entsteht Ozon (aber auch Salpetersäure und andere Stoffe).
Vorkommen und Entstehung von Ozon
Stratosphärisches Ozon
- Hauptartikel: Stratosphärisches Ozon
Die Menge an Ozon in der Atmosphäre wird in Dobson-Einheiten (also pro Erdoberfläche) oder in Parts per million (ppm,also pro Stoffmenge Luft) angegeben. Die höchste Konzentration mit einigen ppm weist Ozon in der Stratosphäre auf. Für seine Entstehung ist dort der Ozon-Sauerstoff-Zyklus verantwortlich. Ozon ist in der Stratosphäre unschädlich und absorbiert teilweise die Ultraviolettstrahlung der Sonne.
Troposphärisches Ozon
- Hauptartikel: Troposphärisches Ozon
In der Atemluft ist Ozon jedoch bereits in weit geringeren Konzentrationen gesundheitsschädlich, insbesondere bewirkt die lokal sehr unterschiedliche Ozonbelastung Reizungen der Atemwege.
Ozonabbau
- Hauptartikel: Ozonabbau in der Stratosphäre
- Hauptartikel: Ozonloch über der Antarktis
- Hauptartikel: Ozonabbau über der Arktis
Literatur
- Katrin Palitzsch, Sabine Göllner, Kristina Lupa, Jörg Matschullat, Corinna Messal, Kirsten Pleßow, Mandy Schipek, Ivonne Schnabel, Christian Weller, Frank Zimmermann: Ozon in Waldökosystemen aus atmosphärenchemischer und pflanzenphysiologischer Sicht. Umweltwissenschaften und Schadstoff-Forschung 17(4), S. 231 - 241 (2005), ISSN 0934-3504
- Georg Erlwein: Über Trinkwasserreinigung durch Ozon und Ozonwasserwerke. Leineweber, Leipzig 1904 (Digitalisat als PDF)
Siehe auch
Weblinks
Lizenzhinweise
|
Dieser Artikel basiert auf dem Artikel Ozon aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |