Kohlenstoffkreislauf: Unterschied zwischen den Versionen
KKeine Bearbeitungszusammenfassung |
|||
| Zeile 8: | Zeile 8: | ||
== Atmosphäre-Ozean == | == Atmosphäre-Ozean == | ||
===Die ozeanische Deckschicht=== | |||
Die gesamte im Ozean gelöste Menge an CO<sub>2</sub> ist 50 Mal größer als der atmosphärische Kohlendioxid-Gehalt und 20 Mal größer als das an Land (Vegetation und Böden) gespeicherte Kohlendioxid. Der Ozen tauscht CO<sub>2</sub> mit der Atmosphäre aus und fungiert bei einer steigenden CO<sub>2</sub>-Konzentration in der Atmosphäre über längere Zeiträume als wichtigte CO<sub>2</sub>-Senke. Der CO<sub>2</sub>-Austausch mit der Atmosphäre findet über die ozeanische Deckschicht statt, die je nach Region zwischen 50-100 m und mehr dick ist und durch die Thermokline abgegrenzt wird, und erfolgt durch Gas-Austausch. Er wird hauptsächlich durch die Differenz im CO<sub>2</sub>-Partialdruck zwischen Ozean und Atmosphäre angetrieben. D.h. bei niedrigerem atmosphärischen CO<sub>2</sub>-Druck gast der Ozean Kohlenstoff in die Atmosphäre aus, bei höherem CO<sub>2</sub>-Druck in der Atmosphäre wird Kohlendioxid im Oberflächenwasser des Ozeans gelöst. Der Austausch umfasst gegenwärtig über 90 Gt C pro Jahr, wobei durch die anthropogene Störung des atmosphärischen Kohlendioxidgehalts 2,2 Gt C mehr vom Ozean aufgenommen als abgegeben werden (bezogen auf die 1990er Jahre). Der Austausch ist regional sehr unterschiedlich. Es gibt Gebiete mit warmem oder aufsteigendem Wasser (vor allem in den Tropen), in denen von Natur aus der Ozean eine Quelle, und andere wie die Ozeane in höheren Breiten, in denen kaltes und salzreiches Wasser absinkt und der Ozean eine Senke ist. | |||
Die für den Austausch zwischen Atmosphäre und Ozean entscheidenden Eigenschaften von Kohlendioxid sind seine leichte Löslichkeit und seine chemische Reaktivität im Wasser. Die Löslichkeit ist bestimmt durch Temperatur, Salzgehalt, Luftdruck, windabhängige Durchmischung u.a. Faktoren, wobei die Temperatur den größten Einfluss besitzt. Wasser mit höherer Temperatur kann weniger Kohlenstoff aufnehmen als Wasser mit geringerer Temperatur. Bei einer Temperaturerhöhung von 1 <sup>o</sup>C steigt der Partialdruck von CO<sub>2</sub> in der ozeanischen Deckschicht über einen längeren Zeiraum (Jahrhunderte) um 7-10 ppm. Je nach Szenario kann bis zum Ende des Jahrhunderts durch diesen Effekt die Gesamtaufnahme von CO<sub>2</sub> um 9–14% geringer ausfallen.3 | |||
Es gibt im Ozean drei Arten von Kohlenstoff: 1. gelöster anorganischer Kohlenstoff (dissolved inorganic carbon = DIC), 2. gelöster organischer Kohhlenstoff (dissolved organic carbon = DOC) und 3. partikular organischer Kohlenstoff (particulate organic carbon = POC). Die überwiegende Mehrheit ist davon gelöster anorganischer, gefolgt vom gelösten organischen Kohlenstoff. DIC, DOC und POC stehen im Verhältnis 2000:38:1. Der gelöste anorganische Kohlenstoff liegt im Ozean überwiegend, d.h. zu 91%, als Hydrogenkarbonat (HCO<sub>3</sub><sup>-</sup>) vor, daneben zu 8% als Karbonat (CO<sub>3</sub><sup>2-</sup>) und zu 1% als physikalisch gelöstes CO<sub>2</sub>. D. h. CO<sub>2</sub> wird bei der Aufnahme aus der Atmosphäre fast vollständig in andere Verbindungen umgewandelt. Das unterscheidet das Kohlendioxid im Ozean grundlegend von dem in der Atmopshäre, wo es keine chemischen Reaktionen eingeht. Im Meer dagegen reagiert CO<sub>2</sub> mit Wassser und Karbonat zu Hydrogenkarbonat (CO<sub>2</sub> + CO<sub>3</sub><sup>2-</sup> + H<sub>2</sub>O = 2 HCO<sub>3</sub><sup>-</sup>). | |||
Durch diese Reaktion mit Kohlendioxid wird im Meer die Karbonat-Konzentration (CO<sub>3</sub><sup>2-</sup>) verringert und die von Hydrogenkarbonat (HCO<sub>3</sub><sup>-</sup>) erhöht. Die Konzentration von Karbonat, das in geringen Mengen aus der Verwitterung an Land über die Flüsse nachgeliefert wird, ist daher eine kritische Größe für die CO<sub>2</sub>-Aufnahmekapazität des Ozeans. Da ein steigender CO<sub>2</sub>-Gehalt der Atmosphäre auch die Aufnahme von Kohlendioxid im Ozean erhöht, wird bei den chemischen Lösungsvorgängen auch mehr Karbonat verbraucht, und es steht zunehmend weniger Karbonat für die chemische Reaktion mit Kohlendioxid zur Verfügung. Seit Beginn der Industrialisierung hat die Karbonatkonzentration durch die Aufnahme des anthropognenen Kohlendioxids bereits um 10% abgenommen. Dadurch verbleibt ein zunehmender Anteil des aufgenommenen Kohlendioxids in seiner ursprünglichen Form im Wasser, und die Möglichkeit des Oberflächenwassers, weiteres Kolendioxid aus der Atmosphäre aufzunehmen, verringert sich. Nach Modellrechnungen würde bei einem Anstieg der athmosphärischen CO<sub>2</sub>-Konzentration auf 750 ppm allein durch diesen Effekt die Aufnahmekapazität des Ozeans um 10% zurückgehen. Eine weitere Bedeutung des Karbonats liegt darin, dass es von etlichen Meeresorganismen gebraucht wird, die für ihre Schalen oder Skelettstrukturen Kalk (Kalziumkarbonat, CaCO<sub>3</sub>) bilden. | |||
Das in der ozeanischen Deckschicht gelöste atmosphärische Kohlendioxid wird aber nicht nur chemisch verwandelt, sondern auch durch die Photosynthese des Phytoplanktons gebunden. Der Kohlenstoff wird dabei in Form von Kohlendioxid oder Hydrogenkarbonat aufgenommen. Das verringert den Partialdruck von CO<sub>2</sub> in der oberen Wasserschicht und fördert damit die Aufnahme von Kohlendioxid aus der Atmosphäre. Die Bruttoprimärproduktion durch das ozeanische Phytoplankton wird auf 103 Gt C pro Jahr geschätzt, die Veratmung (autotrophe Respiration) auf 58 Gt C und die Nettoprimärproduktion entsprechend auf 45 Gt C pro Jahr. Der daraus resultierende und im Phytoplankton gebundene organische Kohlenstoff wird vom Zooplankton konsumiert, wobei durch heterotrophe Respiration 34 Gt C pro Jahr wieder frei gesetzt werden. Der Rest wird direkt oder indirekt zu Abfall (Detritus). | |||
===Der tiefe Ozean=== | |||
== Atmosphäre-Land == | == Atmosphäre-Land == | ||
Version vom 28. April 2008, 19:26 Uhr
Übersicht
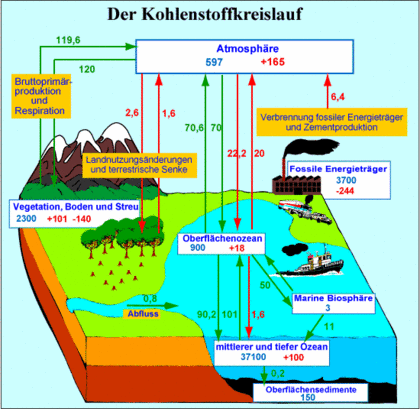
Neben der Atmosphäre sind der Ozean und die Landbiosphäre die wichtigsten Kohlenstoffspeicher, die mit der Atmosphäre in einem aktiven Austausch stehen. Die Landvegetation enthält etwa drei Mal so viel Kohlenstoff wie die Atmosphäre, der Ozean etwa 50 Mal so viel. Die Lithosphäre, die durch Vulkanismus und Verwitterung ebenfalls Kohlenstoff an die anderen Reservoiren abgibt, kann auf Zeitskalen von einigen hundert Jahren wegen der geringen Austauschmengen vernachlässigt werden.
Das atmosphärische CO2 wird relativ schnell mit dem Ozean und den Land-Ökosystemen ausgetauscht. Das Verhältnis zwischen der Aufnahme von atmosphärischem CO2 und der Abgabe an die Atmosphäre durch diese beiden Reservoire bestimmt allgemein das Tempo der Zu- oder Abnahme von Kohlendioxid in der Atmosphäre. Landvegetation und Ozean sind für atmosphärisches Kohlendioxid sowohl Quellen wie Senken. Die Fähigkeit des Ozeans und der Ökosysteme auf dem Land, als Netto-Senken zu wirken, entscheidet darüber, wie viel von dem anthropogen emittierten Kohlendioxid in der Atmosphäre verbleibt. Während der letzten 10 000 Jahre vor 1750 war der Austausch zwischen Atmosphäre und Land sowie Atmosphäre und Ozean relativ ausgeglichen. Die natürlichen Austauschmengen betrugen zwischen Atmosphäre und Land 120 GtC/Jahr und zwischen Atmosphäre und Ozean 90 GtC/Jahr. Das wesentlich größere, allerdings auch sehr langsam reagierende Reservoir des Ozeans steuert den atmosphärischen CO2-Gehalt der Atmosphäre über Zeiträume von Jahrhunderten und Jahrtausenden nachhaltiger als das Landreservoir.
Durch anthropogene Emissionen sind die Austauschprozesse zwischen den drei Reservoiren merklich verändert worden. Dabei tauscht der Ozean von dem anthropogen emittierten Kohlenstoff etwa das Zehnfache der Menge mit der Atmosphäre aus, die zwischen Land und Atmosphäre ausgetauscht wird. Beide Reservoire sind z.Zt. eine Netto-Senke von anthropogenem Kohlenstoff. Die anthropogenen Störungen des natürlichen C02-Kreislaufs resultieren aus zwei Haupt-Quellen: 1. aus der Verbrennung fossiler Energie-Träger und 2. aus Veränderungen der Landnutzung, vor allem der Entwaldung. Von den anthropogenen Emissionen sind etwa 45% in der Atmosphäre verblieben, 30% hat der Ozean aufgenommen, den Rest die Landvegetation. Der Kohlenstoff-Gehalt der Atmosphäre hat durch anthropogene Emissionen seit Beginn der Industrialisierung um 165 GtC oder 38,2% zugenommen. Die Landvegetation hat einen Verlust von 39 GtC (101-140) aufzuweisen, obwohl sie in jüngster Zeit zu einer Nettosenke geworden ist. Der Kohlenstoffgehalt des Ozeans hat sich um 118 GtC erhöht.
Atmosphäre-Ozean
Die ozeanische Deckschicht
Die gesamte im Ozean gelöste Menge an CO2 ist 50 Mal größer als der atmosphärische Kohlendioxid-Gehalt und 20 Mal größer als das an Land (Vegetation und Böden) gespeicherte Kohlendioxid. Der Ozen tauscht CO2 mit der Atmosphäre aus und fungiert bei einer steigenden CO2-Konzentration in der Atmosphäre über längere Zeiträume als wichtigte CO2-Senke. Der CO2-Austausch mit der Atmosphäre findet über die ozeanische Deckschicht statt, die je nach Region zwischen 50-100 m und mehr dick ist und durch die Thermokline abgegrenzt wird, und erfolgt durch Gas-Austausch. Er wird hauptsächlich durch die Differenz im CO2-Partialdruck zwischen Ozean und Atmosphäre angetrieben. D.h. bei niedrigerem atmosphärischen CO2-Druck gast der Ozean Kohlenstoff in die Atmosphäre aus, bei höherem CO2-Druck in der Atmosphäre wird Kohlendioxid im Oberflächenwasser des Ozeans gelöst. Der Austausch umfasst gegenwärtig über 90 Gt C pro Jahr, wobei durch die anthropogene Störung des atmosphärischen Kohlendioxidgehalts 2,2 Gt C mehr vom Ozean aufgenommen als abgegeben werden (bezogen auf die 1990er Jahre). Der Austausch ist regional sehr unterschiedlich. Es gibt Gebiete mit warmem oder aufsteigendem Wasser (vor allem in den Tropen), in denen von Natur aus der Ozean eine Quelle, und andere wie die Ozeane in höheren Breiten, in denen kaltes und salzreiches Wasser absinkt und der Ozean eine Senke ist.
Die für den Austausch zwischen Atmosphäre und Ozean entscheidenden Eigenschaften von Kohlendioxid sind seine leichte Löslichkeit und seine chemische Reaktivität im Wasser. Die Löslichkeit ist bestimmt durch Temperatur, Salzgehalt, Luftdruck, windabhängige Durchmischung u.a. Faktoren, wobei die Temperatur den größten Einfluss besitzt. Wasser mit höherer Temperatur kann weniger Kohlenstoff aufnehmen als Wasser mit geringerer Temperatur. Bei einer Temperaturerhöhung von 1 oC steigt der Partialdruck von CO2 in der ozeanischen Deckschicht über einen längeren Zeiraum (Jahrhunderte) um 7-10 ppm. Je nach Szenario kann bis zum Ende des Jahrhunderts durch diesen Effekt die Gesamtaufnahme von CO2 um 9–14% geringer ausfallen.3
Es gibt im Ozean drei Arten von Kohlenstoff: 1. gelöster anorganischer Kohlenstoff (dissolved inorganic carbon = DIC), 2. gelöster organischer Kohhlenstoff (dissolved organic carbon = DOC) und 3. partikular organischer Kohlenstoff (particulate organic carbon = POC). Die überwiegende Mehrheit ist davon gelöster anorganischer, gefolgt vom gelösten organischen Kohlenstoff. DIC, DOC und POC stehen im Verhältnis 2000:38:1. Der gelöste anorganische Kohlenstoff liegt im Ozean überwiegend, d.h. zu 91%, als Hydrogenkarbonat (HCO3-) vor, daneben zu 8% als Karbonat (CO32-) und zu 1% als physikalisch gelöstes CO2. D. h. CO2 wird bei der Aufnahme aus der Atmosphäre fast vollständig in andere Verbindungen umgewandelt. Das unterscheidet das Kohlendioxid im Ozean grundlegend von dem in der Atmopshäre, wo es keine chemischen Reaktionen eingeht. Im Meer dagegen reagiert CO2 mit Wassser und Karbonat zu Hydrogenkarbonat (CO2 + CO32- + H2O = 2 HCO3-).
Durch diese Reaktion mit Kohlendioxid wird im Meer die Karbonat-Konzentration (CO32-) verringert und die von Hydrogenkarbonat (HCO3-) erhöht. Die Konzentration von Karbonat, das in geringen Mengen aus der Verwitterung an Land über die Flüsse nachgeliefert wird, ist daher eine kritische Größe für die CO2-Aufnahmekapazität des Ozeans. Da ein steigender CO2-Gehalt der Atmosphäre auch die Aufnahme von Kohlendioxid im Ozean erhöht, wird bei den chemischen Lösungsvorgängen auch mehr Karbonat verbraucht, und es steht zunehmend weniger Karbonat für die chemische Reaktion mit Kohlendioxid zur Verfügung. Seit Beginn der Industrialisierung hat die Karbonatkonzentration durch die Aufnahme des anthropognenen Kohlendioxids bereits um 10% abgenommen. Dadurch verbleibt ein zunehmender Anteil des aufgenommenen Kohlendioxids in seiner ursprünglichen Form im Wasser, und die Möglichkeit des Oberflächenwassers, weiteres Kolendioxid aus der Atmosphäre aufzunehmen, verringert sich. Nach Modellrechnungen würde bei einem Anstieg der athmosphärischen CO2-Konzentration auf 750 ppm allein durch diesen Effekt die Aufnahmekapazität des Ozeans um 10% zurückgehen. Eine weitere Bedeutung des Karbonats liegt darin, dass es von etlichen Meeresorganismen gebraucht wird, die für ihre Schalen oder Skelettstrukturen Kalk (Kalziumkarbonat, CaCO3) bilden.
Das in der ozeanischen Deckschicht gelöste atmosphärische Kohlendioxid wird aber nicht nur chemisch verwandelt, sondern auch durch die Photosynthese des Phytoplanktons gebunden. Der Kohlenstoff wird dabei in Form von Kohlendioxid oder Hydrogenkarbonat aufgenommen. Das verringert den Partialdruck von CO2 in der oberen Wasserschicht und fördert damit die Aufnahme von Kohlendioxid aus der Atmosphäre. Die Bruttoprimärproduktion durch das ozeanische Phytoplankton wird auf 103 Gt C pro Jahr geschätzt, die Veratmung (autotrophe Respiration) auf 58 Gt C und die Nettoprimärproduktion entsprechend auf 45 Gt C pro Jahr. Der daraus resultierende und im Phytoplankton gebundene organische Kohlenstoff wird vom Zooplankton konsumiert, wobei durch heterotrophe Respiration 34 Gt C pro Jahr wieder frei gesetzt werden. Der Rest wird direkt oder indirekt zu Abfall (Detritus).
Der tiefe Ozean
Atmosphäre-Land
Siehe auch
| Dieser Artikel ist ein Originalartikel des Klima-Wiki und steht unter der Creative Commons Lizenz Namensnennung-Weitergabe unter gleichen Bedingungen 3.0 Deutschland. Informationen zum Lizenzstatus eingebundener Mediendateien (etwa Bilder oder Videos) können in den meisten Fällen durch Anklicken dieser Mediendateien abgerufen werden und sind andernfalls über Dieter Kasang zu erfragen. |